- Главная
- Оборудование для печатных плат
- Оборудование для поверхностного монтажа
- Технологии производства плат и поверхностного монтажа
- Инструмент для печатных плат и Запасные части
- Материалы и Химикаты для печатных плат и поверхностного монтажа
- Гальваническое оборудование
- Лабораторное и аналитическое оборудование
- Сервис и техническое обслуживание
- Как нас найти
- Начало раздела
- Оборудование
- Поддержка
- Справка
- Контакты
Механизм процессов активирования в технологии химической металлизации
Процессы активирования поверхности диэлектрика перед химической металлизацией с помощью растворов, содержащих благородные металлы, используются в производстве печатных плат с 60-х гг. прошлого века, однако, до настоящего времени в литературе нет подробного объяснения их механизма. Цель настоящей публикации — восполнить этот пробел.
Активирование — одна из важнейших операций в технологии химической металлизации. Сбоям, происшедшим в процессе активирования обязаны своим происхождением такие дефекты, как непрокрытия.
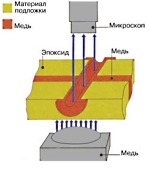
Выявить дефекты непрокрытий сразу после химической металлизации и гальванической затяжки и своевременно принять меры для их устранения позволяет оперативный контроль качества металлизации с помощью визуального осмотра отверстий, расположенных под углом к оптической оси микроскопа. Дополнительную информацию о качестве металлизации дает иллюстрируемый рисунком 1 метод просвечивания ленточных срезов печатных плат (ПП) по сквозным отверстиям (Back Light Test) и осмотр шлифов, выполненных без заливки отверстий эпоксидной смолой (см. рис. 2).
 |
 |
| а)оборудование для просмотра ленточных срезов; | б)ленточный срез сквозного отверстия |
|
Рис. 1. Просвечивание ленточных срезов
|
|
Назначение процесса активирования — инициировать осаждение меди на диэлектрических участках поверхности сквозных отверстий ПП. С этой целью на поверхности диэлектрика создаются каталитически-активные центры, представляющие собой частицы благородного металла (Ag, Au, Pd, Ru, Rh, Pt, Ir, Os). На практике, в процессах активирования чаще всего применяют Pd.
Восстановление меди в растворах химического меднения начинается именно на этих каталитически-активных центрах. Для осаждения на поверхности диэлектрика металлических частиц Pd обычно используют адсорбцию из раствора на границе раздела фаз в сочетании с восстановлением двухвалентного палладия до атомарного состояния.
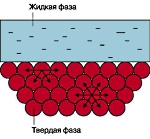
Как известно [1], твердая поверхность, приведенная в контакт с жидкостью, имеет на границе раздела фаз (см. рис. 3) слой молекул (атомов), энергия которых не скомпенсирована силовым полем следующего слоя молекул ввиду его отсутствия. Поэтому поверхностный слой молекул будет стремиться скомпенсировать избыточное силовое поле адсорбцией молекул (атомов) из прилежащей жидкой фазы.
 |
 |
|
Рис. 2. Непрокрытия в сквозном отверстии МПП
|
Рис. 3. Граница раздела фаз
|
В настоящее время известны три способа активирования, в основе которых лежат адсорбционные процессы. Первый способ состоит в последовательной обработке ПП сначала в растворе восстановителя (хлорида двухвалентного олова), а затем в растворе соли двухвалентного палладия. На начальной стадии этого процесса диэлектрическая поверхность адсорбирует соли двухвалентного олова. В ходе промывки плат в воде соли олова гидролизуются с образованием малорастворимых соединений:
Sn2+ + H2O → Sn(OH)+ ↓ + H+
Sn(OH)+ + H2O → Sn(OH)2↓ + H+
При этом силы межмолекулярного взаимодействия между поверхностью диэлектрика и гидроксильными соединениями олова возрастают, так как продукты гидролиза солей олова представляют собой твердые частицы, диспергированные по поверхности на границе раздела фаз и проявляющие свойства коллоидных систем [2]. Поскольку они сами обладают адсорбционной способностью, результирующее межмолекулярное взаимодействие будет складываться из силового поля поверхности и силовых полей частиц.
На заключительной стадии процесса при обработке плат в солянокислом растворе PdCl2 олово и палладий меняются местами. Олово, окисляясь до четырехвалентного, переходит в раствор, а металлический палладий осаждается на поверхности диэлектрика:
Sn(OH)+ + Pd2+ + H+→
→ Pd0 + Sn4+ + H2O;
Sn(OH)2 + Pd2+ + 2H+→
→ Pd0+ Sn4++ 2H2O.
Данный способ активирования имеет существенный недостаток, заключающийся в том, что одновременно на медной поверхности протекает реакция контактного замещения:
Cu + Pd2+ → Cu2+ + Pd0.
Атомарный палладий, осаждаясь на поверхности меди, препятствует ее сцеплению со слоем химически осаждаемой меди и, кроме того, поглощает водород, выделяющийся при реакции восстановления меди в ванне химического меднения. В результате пленка палладия разрыхляется и прочность связи Cu—Cu ослабевает.
Затормозить реакцию контактного замещения помогает замена соли PdCl2 на комплекс двухвалентного палладия с каким-либо лигандом. В присутствии сильного комплексообразующего лиганда, связывающего ионы Pd2+ в прочный комплекс, равновесие в приведенном выше уравнении реакции контактного замещения сдвигается влево, причем тем сильнее, чем больше константа устойчивости комплекса [3]. В этих условиях окислительно-восстановительный потенциал палладия существенно снижается и реакция контактного замещения затормаживается.
Указанный прием положен в основу второго способа активирования, использованного, например, фирмой Atotech (ФРГ) в техпроцессе Neoganth [4].
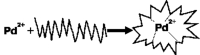
На первой стадии платы обрабатывают в щелочном растворе, содержащем комплекс двухвалентного палладия с органическим хелатообразующим лигандом. Структура подобных комплексов определяется тем, что ион металла при комплексообразовании оказывается со всех сторон окруженным фрагментами органической молекулы, как показано на рисунке 4, а.
Во время обработки происходит селективная адсорбция комплексов палладия на поверхности диэлектрика, к которому молекулы органического лиганда имеют большее сродство, чем к медной поверхности. Реакция контактного замещения на медных участках поверхности в этом способе активирования практически не протекает, поскольку ионы Pd2+ связаны в прочный комплекс с органическим лигандом.
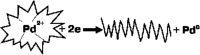
На второй стадии платы обрабатывают в растворе восстановителя, не содержащем хлорида двухвалентного олова. Во время этой обработки комплекс палладия разрушается, а Pd2+ восстанавливается до металла (см. рис. 4, б)
 |
|
а) образование
|
 |
|
б) разрушение
|
|
Рис. 4. Хелатный комплекс палладия
|
При этом твердые частицы металлического палладия, будучи диспергированными по поверхности диэлектрика и обладая значительной адсорбционной способностью, прочно закрепляются на ней. Молекулы органического лиганда переходят в водную фазу и во время операции промывки удаляются с поверхности.
Третий способ состоит в обработке плат в совмещенном растворе активирования — коллоидном растворе, в котором палладий находится в виде уже готовых металлических частиц. Эти частицы остается только нанести и закрепить на поверхности диэлектрика.
В качестве примера в таблице 1 представлен состав совмещенного раствора активирования Cataposit 44, применяемого фирмой Shipley (Великобритания) в техпроцессе химической металлизации Cuposit 200 [5].
| № п/п | Компонент | Содержание, г/л |
|
1.
|
Палладий (в пересчете на PdCl2)
|
0,21...0,24
|
|
2.
|
Олово двухлористое
|
3...6
|
|
3.
|
Кислота соляная
|
0...12
|
|
4.
|
Натрий хлористый
|
190...210
|
|
5.
|
Натрий кислый сернокислый
|
60...70 г/л
|
Таблица 1. Состав раствора Cataposit 44
Физико-химическое исследование состава раствора Cataposit 44 и многолетний опыт приготовления аналогичных растворов из индивидуальных химических веществ дали возможность разобраться в механизме процесса активирования раствором Cataposit 44.
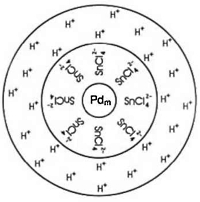
Совмещенный раствор активирования — это типичный лиофобный золь, представляющий собой гетерогенную (двухфазную) систему из дисперсной фазы (твердых коллоидных частиц или мицелл) и дисперсионной среды (водного раствора солей). Центром мицеллы является состоящее из атомарного палладия ядро, которое обычно содержит 6—7 атомов палладия. Вокруг ядра адсорбиционными силами удерживаются катионы двухвалентного олова и хлорид-анионы. В присутствии большого избытка хлорид-анионов двухвалентное олово образует отрицательно заряженные хлоридные комплексы [SnCl4]2-, в результате адсорбции которых на ядре вся частица заряжается отрицательно.Отрицательно заряженные твердые коллоидные частицы отталкиваются друг от друга и равномерно распределяются по всему объему раствора. В результате коллоидный раствор приобретает агрегативную устойчивость (стабильность). Двухвалентное олово в растворе активирования играет роль стабилизатора, удерживая частички металлического палладия от слипания и выпадения в осадок. Обладая восстановительными свойствами, двухвалентное олово предохраняет металлический палладий от окисления.
Вокруг отрицательно заряженной частицы группируются положительно заряженные противоионы — ионы водорода (Н+). Небольшая часть противоионов входит непосредственно в адсорбционный слой коллоидной частицы и расположена на границе раздела двух фаз, остальные противоионы находятся в самой дисперсионной среде и расположены в ней диффузно, то есть на разных расстояниях вокруг отрицательно заряженной коллоидной частицы.
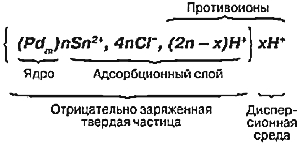
Строение мицеллы раствора активирования можно представить как в виде схемы (см. рис. 5), так и химической формулой (см. рис. 6).
 |
 |
|
Рис. 5. Строение мицеллы палладия в совмещенном растворе активирования
|
Рис. 6. Химическая структура мицеллы палладия в совмещенном растворе активирования
|
В растворе активирования имеется довольно большое количество хлорида натрия (около 200 г/л), необходимое, с одной стороны, для образования отрицательно заряженных хлоридных комплексов двухвалентного олова, а с другой — для создания определенной плотности раствора (1,16 — 1,17 г/см3). При таких значениях плотности на частицы в растворе действует выталкивающая сила, достаточная для того, чтобы воспрепятствовать оседанию коллоидных частиц под действием силы тяжести.
Входящий в состав раствора активирования натрий кислый сернокислый (около 65 г/л) необходим для создания кислой среды, препятствующей гидролизу солей двухвалентного олова.
Соляная кислота требуется для перевода в раствор солей PdCl2 и SnCl2 при приготовлении концентрата, используемого для составления и корректировки раствора активирования.
Концентрат Cataposit 44 Catalyst представляет собой уже готовую коллоидную систему, которую нужно смешать в определенной пропорции с раствором солей. Когда концентрат готовится из индивидуальных солей PdCl2 и SnCl2 • 2H2O, то сначала каждую соль при нагревании растворяют в концентрированной соляной кислоте (8 г PdCl2 в 50 мл кислоты и 240 г SnCl2 • 2H2O в 300 мл кислоты).
Нагретый до 40...45°С раствор соли олова очень быстро приливают к нагретому до той же температуры раствору соли палладия, хорошо перемешивают, прогревают 2—3 часа при 40...45°С и разбавляют водой до 1 литра.
При смешении солянокислых растворов в указанном порядке происходит восстановление палладия по реакции:
Pd2+ + Sn2 + → Pd0 + Sn4+,
и одновременное образование лиофобного золя. Раствор при этом окрашивается в темно-коричневый цвет.
Дисперсность частиц, характеризующая коллоидные системы, находится между молекулярно-дисперсными системами (истинными растворами) и грубодисперсными системами (суспензиями). Для того, чтобы получить стабильный лиофобный золь нужно строго соблюдать условия, при которых достигается необходимое соотношение скоростей: V1 > V2 > V3, где V1 — скорость образования ядер; V2 — скорость роста ядер в объеме; V3 — скорость адсорбции стабилизатора на ядре. Если эти условия не соблюдены, то при смешении исходных компонентов реакция может развиваться как в сторону молекулярно-дисперсных, так и в сторону грубодисперсных систем.
При нарушении указанной выше методики получения золя палладия могут протекать следующие побочные реакции:
- образование окрашенного в зеленый цвет биядерного комплекса [PdCl3(SnCl3)]2-, в котором палладий находится в двухвалентном состоянии [6];
- образование осадка палладиевой черни.
Оба продукта никакого участия в данном способе активирования не принимают, а только увеличивают потери драгметалла.
В реакции восстановления палладия участвует около 4% от всего количества добавленного хлорида двухвалентного олова. Остальное количество двухвалентного олова необходимо для создания и стабилизации коллоидной системы.
Образовавшиеся за счет реакции восстановления частички металлического палладия слипаются, укрупняются и стремятся выпасть в осадок. Двухвалентное олово адсорбируется на ядре в виде отрицательно заряженных комплексных анионов и приостанавливает рост ядра. К моменту, когда произойдет адсорбция стабилизатора, ядро успевает вырасти до размера 6—7 атомов Pd.
После получения коллоидной системы ее, также как и при использовании фирменного концентрата, смешивают в необходимой пропорции с водным раствором солей.
Цель получения раствора активирования в коллоидной форме заключается в следующем. Коллоидные растворы высокодисперсные системы. Диаметр частиц в них составляет 10-5...10-7 см. При таком диспергировании значительно возрастает как удельная поверхность дисперсной фазы, так и поверхностная энергия молекул, лежащих на границе раздела фаз. Избыток свободной энергии заставляет коллоидную систему стремиться к ее уменьшению, например, за счет адсорбции. Таким образом, получение раствора активирования в коллоидной форме — это получение палладиевых частиц, обладающих значительной адсорбционной способностью.
Поскольку диэлектрическая поверхность имеет отрицательно заряженные группы как на стекле, так и на смоле, то адсорбция отрицательно заряженных мицелл палладиевого катализатора становится возможной только после предварительной подготовки (модификации) поверхности. Такая модификация достигается обработкой плат в растворе кондиционера, содержащего поверхностно-активное вещество (ПАВ) неионогенного или катионного типа. Адсорбция ПАВ на диэлектрических участках поверхности экранирует (или нейтрализует) отрицательные заряды стекла и смолы, обеспечивая тем самым адсорбцию палладиевых частиц.
В то же время, почти не происходит адсорбции мицелл палладиевого катализатора на поверхности медной фольги. Связано это с тем, что около положительно заряженной медной поверхности в присутствии высокой концентрации хлоридов (около 200 г/л NaCl) возникает двойной электрический слой — своеобразный конденсатор, внешняя обкладка которого заряжается отрицательно [1] и электрофоретически отталкивает отрицательно заряженные палладиевые частицы.
Самопроизвольное снижение свободной энергии коллоидной системы происходит на всем протяжении ее использования и проявляется в старении коллоидного раствора. По мере эксплуатации раствора активирования непрерывно и необратимо идет процесс агрегирования (слипания, укрупнения) коллоидных частиц. Это происходит потому, что противоионы из дисперсионной среды постепенно за счет сил притяжения все ближе подходят к границе раздела фаз и перемещаются в адсорбционный слой. Доля x в уравнении, приведенном на рисунке 6, уменьшается, а (2n - x) — возрастает. Когда х станет равным 0, количество ионов положительного и отрицательного знака в адсорбционном слое будет одинаковым. Такие потерявшие заряд частички будут слипаться и укрупняться.
Старение коллоидного раствора активирования проявляется и в том, что двухвалентное олово постепенно окисляется кислородом воздуха до четырехвалентного, которое стабилизирующим действием не обладает.
При длительной эксплуатации раствора активирования в нем происходит также накопление нежелательных примесей, в первую очередь, меди за счет растворения окислов меди в кислом растворе:
CuO + 2H+ → Cu2+ + H2O.
Максимально допустимая концентрация двухвалентной меди в растворе активирования — 2 г/л.
Когда платы опускают в раствор активирования, то на диэлектрических частях поверхности начинают адсорбироваться отрицательно заряженные коллоидные частицы, количество которых определяется временем обработки. Часть олова, находящаяся под ядром палладия, непосредственно связывается с поверхностью межмолекулярными силами. Другая часть олова с поверхностью не связана и экранирует палладиевые центры. Поэтому перед химическим меднением необходима еще одна стадия, во время которой олово, экранирующее палладиевые центры, удаляют. Для этого платы обрабатывают в растворе ускорителя. Ввиду амфотерности соединений двухвалентного олова в качестве ускорителя пригодны как кислые, так и щелочные растворы.
В процессе Cuposit 200 фирмы Shipley используется раствор Accelerator 19H (см. табл. 2).
|
№п/п
|
Компонент
|
Содержание
|
|
1.
|
Борфтористоводородная кислота (d — 1,27)
|
0,25 — 0,27N
|
|
2.
|
Глицерин (d — 1,26)
|
3...5 мл/л
|
Таблица 2. Состав раствора Accelerator 19H
Борфтористоводородная кислота растворяет олово, не связанное с поверхностью, в соответствии с уравнением реакции
[SnCl4]2- + 2HBF4 →
Sn(BF4)2 + 2H+ + 4Cl-,
и обнажает палладиевые центры. Раствор работает в очень узком интервале по кислотности (0,25 — 0,27 N). Если нормальность будет ниже 0,25, то часть олова так и останется на поверхности и будет экранировать палладиевые центры. Если же нормальность превысит 0,27, борфтористоводородная кислота растворит и то олово, которое связано с поверхностью, а вместе с ним удалятся и палладиевые центры. И тот и другой вариант приведет к непрокрытиям на стадии химического меднения.
Еще одно назначение раствора ускорения — удалить с медных торцов внутри сквозного отверстия, а также с поверхности ПП те частички палладиевого катализатора, которые все же смогли адсорбироваться на медной фольге.
При обработке плат в растворе ускорителя поверхность медной фольги подтравливается и вместе с медью удаляется палладий. Глицерин, как комплексообразующее вещество, связывает ионы меди в прочный комплекс. В результате окислительно-восстановительный потенциал меди сдвигается в отрицательную область, что способствует ее растворению в борфтористоводородной кислоте.
ЛИТЕРАТУРА
- Киреев В.А. Курс физической химии. М: Химия, 1989, стр. 480, стр. 561.
- Фридрихсберг Д.А. Курс коллоидной химиии. СПб: Химия, 1995, стр. 11.
- Отто М. Современные методы аналитической химии. М: Техносфера, 2003, т.1 стр. 115.
- Vertical PTH Electroless Copper Process. Проспект фирмы Atotech на выставке EXPO Electronica, апрель 2006г.
- Advances in MLB Technology. Cuposit 200 PTH Process, 1988 г.
- Алимарин И.П., Бирюков А.А., Шленская В.И. Вестник МТУ, Химия, 1967, (№5), стр. 91.




